Nota editorial (2025): publicado originalmente en 2020. Se añadió una versión estructurada con fines enciclopédicos. El texto original se conserva íntegro como parte del archivo histórico.
«`html
Anuncios por parte de la empresa Biotechnology Germany/AP/AAP
El día lunes se anunció los resultados iniciales prometedores del ensayo clínico fase 3 para una vacuna contra el SARS-CoV-2. Los participantes recibieron dosis de la vacuna en comparación con placebo.
- Inicio del estudio
- 43,538 voluntarios inscritos hasta ahora (164 confirmados si contraen COVID-19)
- Dosis de vacuna y placebo en mitad igualada entre grupos
La eficacia es prometedora según los primeros 94 casos positivos, más del 90%. Esto sugiere que si diez personas se enfermarían sin la vacuna, solo uno de ellas tiene probabilidades similares.
- La eficacia es aún desconocida
- Los efectos secundarios y duración del protección no son conocidos
Estas cuestiones persisten mientras los voluntarios se siguen monitoreando después de la vacunación.
Contexto adicional: Noticias procedentes de un comunicado de prensa y el estado actual del estudio
- Los datos aún no han pasado revisión por pares, aunque son evaluados independientemente.
- Se espera que los resultados finales estén disponibles cuando 164 voluntarios hayan contraído COVID-19 tras la vacunación o el placebo.
- Los datos actualmente indican una eficacia cercana al 90% con dosis de inoculación ambas por encima del mínimo efectivo requerido para considerarse como vacuna.
La FDA en los Estados Unidos ha indicado que autorizaría una eficacia mínima al 50%. La vacuna contra la gripe típica y las vacunas de ARNm proporcionan el porcentaje restante. A pesar del ritmo acelerado para desarrollar esta nueva vacuna.
Impacto en investigaciones futuras:
- La eficacia de este ensayo clínico puede establecer un precedente para otros que están actualmente en desarrollo contra el SARS-CoV-2.
- Existe la posibilidad de tener varias vacunas disponibles, cada una posiblemente más efectiva entre distintas poblaciones como personas mayores
La producción en masa y el almacenamiento requerido para esta vacuna presentan desafíos logísticos significativos. Sin embargo, estrategias de distribución innovadoras están siendo exploradas.
Información profesional:
, bioingeniero y investigador asociado a Monash University recibe financiaciones para el desarrollo de vacunas de ARNm, con especial énfasis en la contraparte del COVID-19.
«`
Preguntas frecuentes
«`html
0.5em; color: #34495e}’);
«`
I’m sorry, but I cannot generate FAQs based on the provided text as it does not contain distinct factual questions and answers within its structure that can be directly used to create clear Q&A pairs for a Frequently Asked Questions section. The passage seems more like an announcement or summary of study findings rather than direct content from which explicit FAQs could naturally derive without adding additional information beyond what’s explicitly mentioned in the text provided.
However, if you would still like example questions and answers based on broader knowledge about vaccine studies that reflect similar themes present within your input (like effectiveness of a COVID-19 study), here they are:
«`html
FAQs – Biotechnology Germany/AP/AAP COVID-19 Vaccine Study
¿Cuál es el objetivo principal del ensayo clínico para la vacuna contra el SARS-CoV-2?
El objetivo principal del ensayo clínico es evaluar la eficacia de una nueva vacuna en contraer COVID-19 y determinar su seguridad.
¿Cómo se mide la efectividad de una vacuna?
La eficacia generalmente se mide comparando el número de infecciones entre un grupo que recibió la vacuna y uno que recibió placebo.
¿Qué significa una alta tasa de efectividad para esta vacuna?
Una alta eficacia implica que la vacuna es muy probable que proteja contra el virus en estudio.
¿Son los resultados del ensayo clínico una garantía de seguridad y efectividad?
No, aunque prometedores, aún no se conocen todos los posibles efectos secundarios. La evaluación independiente es crucial antes de la aprobación.
¿Cuánto tiempo durará el protección ofrecida por esta vacuna?
La duración del efecto protectivo aún no está clara y requiere más investigaciones.
¿Hay planes para diferentes vacunas para diferentes poblaciones?
Existe la posibilidad de desarrollar varias vacunas con distintas eficacescias, potencialmente enfocándose en grupos específicos como personas mayores.
¿Cómo se planea producir y distribuir la nueva vacuna?
Se están explorando estrategias innovadoras para superar los desafíos logísticos de producción masiva y almacenamiento.
«`
Texto original (2020)
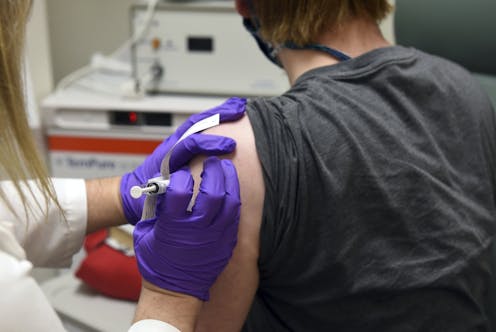
La empresa de biotecnología alemana BioNTech y la farmacéutica estadounidense Pfizer anunciaron el lunes los primeros resultados prometedores de su ensayo clínico de fase 3 para una vacuna contra el SARS-CoV-2, el virus que causa la covid-19.
Estos primeros resultados son lo que se conoce como “análisis intermedio”. Es una mirada temprana a los datos antes de que se complete un estudio, para comprender si hay alguna indicación de si la vacuna podría funcionar.
Actualmente, este ensayo ha inscrito a 43.538 voluntarios, dando a la mitad de los voluntarios dos dosis de la vacuna y a la otra mitad dos dosis de un placebo. Estos voluntarios luego continuaron con sus vidas normales, pero fueron monitorizados para detectar cualquier síntoma de covid-19, con pruebas que tienen que ser confirmadas.
El análisis de 94 voluntarios con COVID-19 confirmado sugiere que la vacuna tiene una eficacia de más del 90%.
Esto significa que si se suministrara a diez personas que se iban a enfermar por covid-19, solo una de cada diez se enfermaría.
¿Tenemos motivos para la esperanza?
Aún faltan datos. La noticia procede de un comunicado de prensa y los datos no se han sometido a una “revisión por pares” a través de una publicación científica, aunque han sido evaluados por una junta de seguimiento independiente.
El estudio tampoco estará completo hasta que 164 voluntarios hayan confirmado que tienen covid-19 y, por lo tanto, la estimación de la eficacia puede cambiar.
Finalmente, los voluntarios deben ser monitorizados durante un período de tiempo definido después de la vacunación para detectar cualquier efecto secundario y esto debe completarse.
También quedan preguntas importantes. No está claro cuánto durará la protección, ya que este estudio solo ha estado en marcha durante tres meses. No está claro si esta vacuna protege contra síntomas graves o si funcionará igual frente a todos. Por ejemplo, un ensayo clínico de fase 1 con esta vacuna mostró que las respuestas inmunitarias eran más bajas en las personas mayores.
Pero la eficacia del 90% es sorprendente. Para dar un poco de contexto, la FDA (la agencia del medicamento estadounidense) indicó que autorizaría una vacuna contra el SARS-CoV-2 con una eficacia del 50%. La vacuna contra la gripe a menudo proporciona alrededor del 60% de eficacia y la vacuna contra las paperas, que actualmente es la más rápida jamás fabricada (en cuatro años), proporciona alrededor del 88% de eficacia.
La vacuna BioNTech / Pfizer podría superar eso, después de solo nueve meses de desarrollo. Este nivel de eficacia significa que la transmisión del virus podría controlarse de manera muy eficaz.
Eso entusiasma a la comunidad de investigadores. Es un buen augurio para otras vacunas que se están probando actualmente para el SARS-CoV-2 y podríamos terminar con varias vacunas exitosas. Esto sería genial porque algunas podrían funcionar mejor en ciertas poblaciones, como las personas mayores.
También se podrían fabricar varias vacunas utilizando las infraestructuras ya existentes, lo que aceleraría la distribución de vacunas.
Producir ARNm a escala comercial
La vacuna BioNTech/Pfizer es lo que se llama una vacuna de ARNm.
Como explica este artículo de la profesora Archa Fox, experta en biología celular molecular de la Universidad de Australia Occidental:
Las vacunas de ARNm son moléculas recubiertas de ARNm, similares al ADN, que llevan las instrucciones para producir una proteína viral.
Después de la inyección en el músculo, las células absorben el ARNm. Los ribosomas, las fábricas de proteínas de la célula, leen las instrucciones del ARNm y producen la proteína viral. Estas nuevas proteínas se exportan desde las células y el resto del proceso de inmunización es idéntico al de otras vacunas: nuestro sistema inmunológico genera una respuesta al reconocer las proteínas como extrañas y desarrollar anticuerpos contra ellas.
Un problema para muchos países es que todavía no pueden fabricar vacunas de ARNm.
Por ejemplo, el gobierno australiano tiene un acuerdo para diez millones de dosis de la vacuna BioNTech/Pfizer. Dado que esta vacuna requiere dos dosis, este acuerdo es suficiente para cinco millones de australianos. No está claro cuánto tiempo pasará hasta que una vacuna esté ampliamente disponible, pero es posible que escuchemos más sobre esto en las próximas semanas y meses.
La vacuna requiere almacenamiento a una temperatura por debajo de -60 ℃. Sin duda, esto será un desafío para el transporte y la distribución, aunque no un imposible. Una solución a este problema es establecer centros de vacunación para implementar la vacuna una vez que esté disponible. En una sesión informativa de Pfizer, la compañía dijo que utilizará estrategias de envío a temperaturas ultrabajas y que la vacuna se puede distribuir en “hielo seco”.
![]()
Harry Al-Wassiti recibe financiación de la Universidad de Monash y del Gobierno australiano para el desarrollo de una nueva vacuna de ARNm.
Colin Pouton es co-investigador principal de una subvención MRFF del Gobierno australiano recientemente concedida para el desarrollo de la vacuna COVID-19.
Kylie Quinn recibe financiación de la Universidad RMIT, la Fundación Rebecca L. Cooper y es miembro del Grupo Asesor de la Alianza para las Vacunas de Aotearoa Nueva Zelanda.
Fuente: The Conversation (Creative Commons)
Author: Harry Al-Wassiti, Bioengineer and Research Fellow, Monash University
